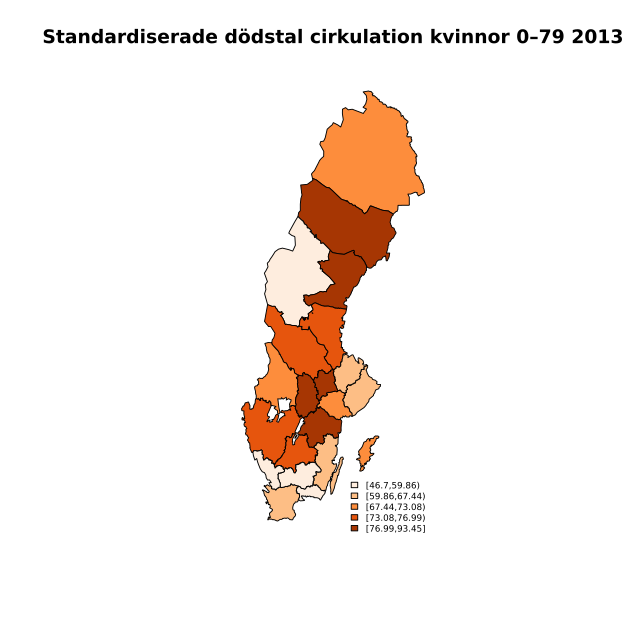
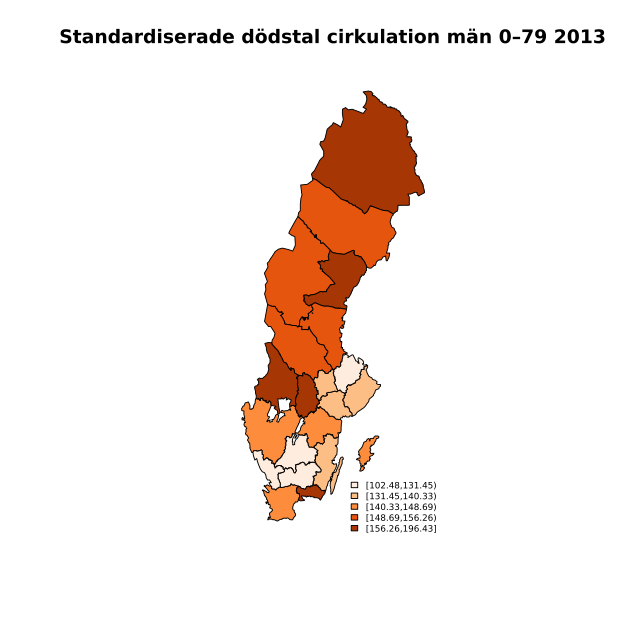
I förra inlägget påpekade jag att en studie som Huxley m.fl. (2015) inte kunde användas för att visa det SVT påstod att den visade: att kvinnor med typ 1-diabetes har högre dödlighet än män med typ 1-diabetes. En studie som däremot är relevant för detta är den finska Forssas m.fl. (2013), där forskarna studerat åldersspecifika dödstal hos kvinnor och män i Finland. De har använt sig av data från flera olika finska register och har avgränsat ”insulinbehandlad diabetes” på ett sätt som de anser ringar in typ 1-diabetes ganska väl (kontinuerlig insulinbehandling och inga läkemedel för att öka bukspottskörtelns insulinsekretion). I fortsättningen använder jag i detta inlägg ”typ 1-diabetes” för att referera till insulinbehandlad diabetes.
Ett resultat är att typ 1-diabetes mycket riktigt är en starkare riskfaktor bland kvinnor (åldersstandardiserade dödstal relativt icke-diabetiker i åldern 1–79 år under perioden 2003–07 4,29; 95-procentigt konfidensintervall 4,08–4,51) än bland män (3,45; 3,31–3,58). Men i artikeln finns grafer som visar utvecklingen av dödlighet totalt och i cirkulationssjukdom, tumörer och övriga orsaker efter ålder bland kvinnor och män från 30-årsåldern upp till över 80 års ålder för åren 2002–03. I supplementet S1 redovisas dessutom dessa uppgifter för perioderna 1998–2002 och 2003–07 i 15-åriga åldersintervall från 0–14 till 60–74 år, med 75– år som öppet intervall. Av såväl graferna som supplementet framgår att kvinnor med typ 1-diabetes inte har högre dödstal än män i någon ålder. Den större dödlighetsökningen bland kvinnor är inte tillräcklig för att uppväga den markant lägre dödligheten bland kvinnor utan diabetes.
De uppgifter som framställdes av SVT, att personer med typ 1-diabetes skulle ha minst tiofaldigt ökade dödstal, eller ”ökad risk att dö i förtid”, jämfört med övriga befolkningen, verkar också klart överdrivna för befolkningen som helhet, vilket är i linje med aktuella metaanalyser, som jag påpekade i förra inlägget. Dock framgår av Forssas m.fl. (2013) också en interaktion mellan ålder och diabetes när det gäller effekt på dödlighet. Hos såväl diabetiker som icke-diabetiker ökar dödstalen exponentiellt med stigande ålder. Men de logaritmiska kurvorna är brantare bland icke-diabetiker, så de relativa skillnaderna i dödstal mellan diabetiker och icke-diabetiker är mindre bland äldre personer; ett exempel på det s.k. Strehler–Mildvansambandet. Bland kvinnor i 30-årsåldern med typ 1-diabetes är den totala dödligheten nästan tio gånger så hög som bland jämnåriga kvinnor utan diabetes.
När det gäller dödlighet i cirkulationssjukdom är de relativa ökningarna ännu större; kvinnor med typ 1-diabetes i åldersintervallen 30–44 och 45–59 år har 10–15 gånger så höga dödstal som kvinnor i motsvarande åldrar utan diabetes. De har också 3–4 gånger så höga dödstal i tumörer och 6–7 gånger så höga dödstal i övrig dödlighet (infektioner, endokrina sjukdomar, vilket inkluderar de fall där diabetes i sig rapporteras som dödsorsak, njursjukdomar etc.). Det är dock knappast klart i alla dessa fall vad som är en följd av diabetes och vad som speglar omvänd kausalitet eller confounding.
Det är inte heller klart hur livstidssannolikheten för död genom olika orsaker skiljer sig mellan diabetiker och övriga befolkningen. Jag försökte mig på att konstruera en livslängdstabell för kvinnor med typ 1-diabetes 2007 med relativa dödstal i cirkulationssjukdom, tumörer och övriga orsaker beräknade utifrån uppgifterna för 2003–07 i S1, tillsammans med uppgifter om dödsorsaksfördelningen i 5-åriga åldersintervall i allmänbefolkningen från WHO (2014) och livslängdstabeller från Human Mortality Database (2014). Jag sökte också beräkna fördelningen av dödsorsaksgrupperna. Tillvägagångssättet var, grovt, följande.
- Beräkna dödstal \(m_{\text{Cirk}}(x,\text{a}),m_{\text{Tum}}(x,\text{a}),m_{\text{Övr}}(x,\text{a})\) för allmänbefolkningen i ålder \(x\).
- Beräkna dödstal \(m_{\text{Cirk}}(x,\text{d}),m_{\text{Tum}}(x,\text{d}),m_{\text{Övr}}(x,\text{d})\) för diabetiker i åldern \(x\) utifrån uppgifter om relativa tal baserade på S1.
- Beräkna total dödlighet för diabetiker \(m(x,\text{d})\) genom att summera dödstalen i ovanstående punkt. Konstruera en livslängdstabell utifrån detta (som beskrivs i dokumentationen till Human Mortality Database (2014)).
- Beräkna andelen diabetiker som dör av t.ex. cirkulationssjukdom vid ålder \(x\) genom \(d(x,\text{d})\times(m_{\text{Cirk}}(x,\text{d})/m(x,\text{d}))\) (där \(d(x,\text{d})\) är andelen diabetiker som dör av någon orsak vid \(x\)).
- Summera dessa andelar över åldrarna.
Ett resultat är att kvinnorna med typ 1-diabetes skulle ha en förväntad återstående livslängd på 41,7 år vid 30 års ålder, att jämföra med 53,5 år för finska kvinnor i allmänhet. Bland 30-åriga kvinnor i allmänbefolkningen skulle 19 procent förr eller senare dö av tumörer och 46 procent av cirkulationssjukdomar, och bland kvinnor med typ 1-diabetes är dessa andelar 23 och 42 procent.
De specifika resultaten måste tas med en nypa salt, då det finns flera osäkerhetskällor. Men det illustrerar att det inte behöver vara så att de som exponerats för en riskfaktor \(X\) för en viss dödsorsak \(C\) har högre livstidssannolikhet för död genom \(C\) än de som inte exponerats – inte ens om \(X\) i alla åldrar är en starkare riskfaktor för \(C\) än för annan dödlighet. Detta är uppfyllt när det gäller cirkulationssjukdom och typ 1-diabetes bland kvinnor i alla åldersintervall över 30 år. Ändå är det en något mindre andel av dessa kvinnor som skulle dö av cirkulationssjukdom jämfört med befolkningen i övrigt. Skälet är att dödligheten i cirkulationssjukdom bland kvinnor är koncentrerad till de högsta åldersgrupperna, och att många kvinnor med typ 1-diabetes skulle dö av andra orsaker innan de nådde dit.
Referenser
Forssas, Erja, Reijo Sund, Kristiina Manderbacka, Martti Arffman, Pirjo Ilanne-Parikka, och Ilmo Keskimaki. 2013. ”Increased cancer mortality in diabetic people treated with insulin: A register-based follow-up study”. BMC Health Services Research 13 (1): 267. doi:doi:10.1186/1472-6963-13-267.
Huxley, Rachel R., Sanne A. E. Peters, Gita D. Mishra, och Mark Woodward. 2015. ”Risk of all-cause mortality and vascular events in women versus men with type 1 diabetes: A systematic review and meta-analysis”. The Lancet Diabetes & Endocrinology (2015/02/06). doi:doi:10.1016/S2213-8587(14)70248-7.
University of California, Berkeley, och Max Planck Institute for Demographic Research. 2014. ”Human Mortality Database”. http://www.mortality.org/.
WHO. 2014. ”WHO Mortality Database”. http://www.who.int/healthinfo/mortality_data/en/index.html.